В САЩ са притеснени относно бъдещето на електроконвулсивната терапия 02 февруари 2011
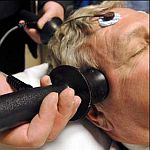
Съветен комитет към Американската администрация по храните и лекарствата (FDA) препоръча електроконвулсивната терапия да запази своя клас III рисков статус. Това породи страхове в Американската Психиатрична Асоциация (АПА) относно бъдещето на може би единствената терапия на тежка и резистентна депресия и други сериозни ментални заболявания.
Ако FDA реши да послуша съвета на Комисията по Неврологични Устройства, това означава, че 2 компании, които произвеждат ЕКТ устройства, ще имат 30 месеца да предоставят постмаркетингови данни, че устройствата са безопасни и ефективни.
Психиатрите се притесняват относно несигурността във финансирането на бъдещи ЕКТ проучвания и дали въобще провеждането на такива би убедило последващ съветен комитет.
В становище, пуснато 2 дни след решението на съветната комисия, от AПА се надяват, че ЕКТ ще продължи да бъде достъпна като терапевтична опция при пациенти с тежки психиатрични заболявания.
ЕКТ е подходяща за малък процент пациенти, главно лица с тежки ментални заболявания, неотговарящи на конвенционална терапия. Използвана според настоящите ръководства и от добре трениран психиатър, ЕКТ е изключително безопасна и ефективна, обяснява д-р Бернщтайн, президент на АПА.